Su ve +4 °C Önemi
Su neden üsten donar? Denizler, göller üstten donmasa ne olurdu?
Su (H2O) tüm canlıların yaşam kaynağıdır. Yaşamın başlaması su sayesinde olmuştur, devam etmesini de su sağlamaktadır. Su bizim vazgeçilmez yaşam kaynağımız ve aynı zamanda çok farklı özelliklere sahip kimyasal bir bileşiktir. Su moleküllerini diğer moleküllerden ayırt eden birçok özellik vardır. Bunlardan bir tanesi diğer moleküllerin katı halleri daha yoğun olduğu için sıvı hallerinin dibine çökerken suyun katı hali olan buzun, suyun üzerinde yüzmesidir. Peki su moleküllerinin diğer moleküllerden farklı olmasını sağlayan şey nedir?
Suyun özkütlesinin sıcaklığa bağlı olarak özel bir durumu vardır. Suyun özkütlesi, 0 °C’den +4 °C’ye doğru artar ve en yüksek değeri olan 1 g/cm3 e ulaşır. +4 °C’den sonra özkütlesi düşmeye başlar. Suyun özkütlesi +4 °C ve 1 atm basınç altında 1000 kg/m3 tür (1 g/cm3). Su dışındaki sıvıların çoğunun katı hâlinin özkütlesi, kendi sıvı hâllerinin özkütlesinden daha büyüktür. Bu nedenle katı hâlleri sıvı hâllerinde yüzemez, dibe batar. Ama su için durum farklıdır. Moleküler yapısı nedeniyle su donduğunda hacmi büyüyen nadir maddelerden biridir.
Diğer kimyasal maddelerin (element ve bileşikler) atomları veya molekülleri soğudukça birbirine yaklaşır ve yoğunlaşır. Su molekülleri de soğudukça birbirine yaklaşır fakat en büyük yoğunluğa +4 °C’ ye geldiğinde ulaşır. Yani su moleküllerinin en yoğun olduğu hal katı hali değildir, +4 °C’deki (normal koşullarda 1 atm basınç altındaki) sıvı halidir.
Muhtemelen suyun bu farklı özelliğini birçoğunuz gözlemlemişsinizdir. Örneğin, buzluğa koyduğunuz su şişesi donduğu zaman çatlar çünkü hacmi artmıştır. d=m/v formülünden hacim (v) ve özkütlenin (d) ters orantılı olduğunu düşünürsek donan maddenin molekülleri birbirine yaklaşarak hacmi azalacak ve özkütlesi yani yoğunluğu artacaktır.Ama su molekülleri böyle davranmaz. Su molekülleri donarken birbirinden uzaklaşarak hacmi artar ve şişeyi çatlatır. Başka bir örnekte ise, kışın göllerde ya da su birikintilerinde buzların su üzerinde yüzdüğünü görmüşsünüzdür. Yoğunluğu daha az olan katı haldeki su molekülleri yani buz, sıvısının üzerinde yüzmektedir.
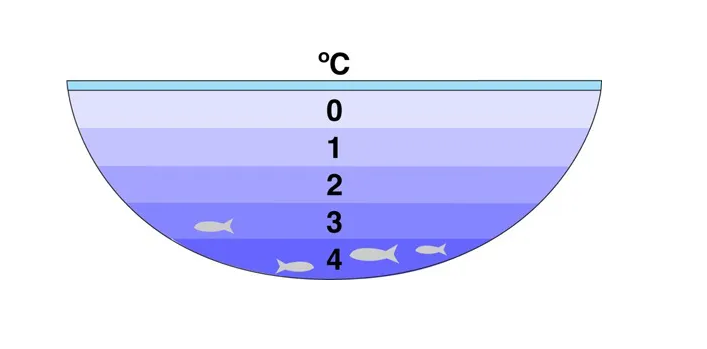
Su dipten değil de tepeden donmaya başlar. Buz su yüzeyinde kalır çünkü yoğunluğu sudan daha azdır. Bu yüzden donmuş göllerde balıklar ve diğer canlılar suyun sıvı olduğu yerlerde yaşayabilir. Eğer su için durum bu şekilde olmasaydı deniz, göl ve nehirlerde canlı hayat devam edemezdi.
Su molekülleri sıvı haldeyken rastgele form alırken buz halindeyken kristal kafesler oluşturarak hizaya girerler. Su moleküllerini bir arada tutan hidrojen bağları bu kristal kafeslerin oluşmasını sağlar. Bu formu alırken moleküller sıvı hale göre daha çok hacim kaplar, bu yüzden aynı miktardaki buzun hacmi sıvı halinden daha fazla olur. Buz halindeki moleküllerin en bilindik formu altıgen (Hegzagonal ) yapıda olanıdır. Moleküllerin altıgen şeklini aldığı buz formu nispeten daha yayılmış bir yapıya sahiptir; hacmi daha fazla, yoğunluğu daha küçüktür. Altıgen terimi, kristalin düzlemine bakıldığında oluşan kristal yapıdan gelir. +4 °C’den büyük sıcaklıklarda, moleküllerin termal hareketi ile birlikte hidrojen bağları kırılarak yeni formlara dönüşürler. Bu durumda, sıcaklık arttıkça yayıldıkları hacim artar dolayısıyla yoğunlukları azalır. Bu, tüm sıvılarda görülen davranışlardan biridir.

